Антитромботическая терапия при ИБС. Антиагреганты при ишемической болезни сердца: состояние проблемы
- Антитромботическая терапия при ИБС. Антиагреганты при ишемической болезни сердца: состояние проблемы
- Антитромботическая терапия рекомендации 2020. Ведение пациентов с фибрилляцией предсердий и острым коронарным синдромом
- Двойная антитромбоцитарная терапия после инфаркта. Сохраняющийся риск сосудистых осложнений и эффективность длительной двойной антитромбоцитарной терапии после инфаркта миокарда
- Двойная антитромбоцитарная терапия после стентирования. Продолжительность двойной антитромбоцитарной терапии: спорные вопросы и возможные решения
- Двойная антиагрегантная терапия при окс. Обзор
- Двойная антиагрегантная терапия при инсульте. Инсульт и ТИА
Антитромботическая терапия при ИБС. Антиагреганты при ишемической болезни сердца: состояние проблемы
.В.В.Косарев, С.А.Бабанов
ГОУ ВПО «Самарский государственный медицинский университет»
Ишемическая болезнь сердца (ИБС), являющаяся одной из важнейших медицинских проблем XXI века, известна человечеству на протяжении многих столетий. Еще в 1772 г. английский врач У.Геберден (W.Heberden) в своем докладе Лондонскому Королевскому обществу подробно и точно охарактеризовал клиническую картину грудной жабы (геберденова грудная жаба - angina pectoris): «…У тех, кто подвержен ей , при ходьбе, особенно после еды, возникают болезненные, наиболее неприятные ощущения в груди, которые, кажется, отнимут жизнь, если только усилятся или продолжатся, но стоит остановиться, как эта скованность исчезает. Во всех других отношениях пациенты в начале этой болезни чувствуют себя хорошо и, как правило, отсутствует укороченное дыхание, от которого это состояние полностью отличается». Геберден отмечал, что стенокардия может возникнуть при дефекации, волнении, в покое, в положении лежа; зимой заболевание протекает тяжелее, чем летом, и им чаще болеют пожилые мужчины с избыточной массой тела; описывал иррадиацию боли в левую руку и случаи внезапной смерти во время приступа. В 1909 г. на I съезде российских терапевтов было дано классическое описание клинической картины инфаркта миокарда (ИМ) в докладе выдающихся русских терапевтов В.П.Образцова и Н.Д.Стражеско «К симптоматологии и диагностике тромбоза коронарных артерий». В настоящее время в начале XXI века тромботические осложнения атеросклероза (ИБС, ИМ, инсульт) являются ведущими среди заболеваний, характеризующих фенотип современного больного, наряду с сахарным диабетом и хронической обструктивной болезнью легких. Ежегодно в Российской Федерации от сердечнососудистых заболеваний умирают более 1 млн человек, т.е. примерно 700 человек на 100 тыс. населения. ИБС часто развивается у трудоспособных, творчески активных лиц, существенно ограничивая их социальную и трудовую активность, усугубляя социально-экономические проблемы в обществе .
Антитромботическая терапия рекомендации 2020. Ведение пациентов с фибрилляцией предсердий и острым коронарным синдромом
С результатами классических исследований, касающихся двойной и тройной антитромботической терапии, слушатели симпозиума ознакомились по докладам профессоров Д. А. Затейщикова, руководителя первичного сосудистого отделения ГКБ № 51 (Москва), и Peter R. Sinnaeve из Левенского университетского госпиталя (Бельгия). Внутренние протоколы ведения пациентов с острым коронарным синдромом (ОКС) и ФП в передовых отечественных медицинских учреждениях оказались соответствующими актуальным европейским рекомендациям.
Известно, что терапия этих состояний не является взаимозаменяемой, на одной чаше весов всегда находится риск тромбоза стента и повторного инсульта или инфаркта, на другой – риск серьезных кровотечений. Имеющиеся рекомендации зачастую могут быть противоречивы и недостаточно понятны. К счастью, эра ПОАК ознаменовалась целой серией основополагающих исследований: PIONEER AF-PCI (ривароксабан), RE-DUAL PCI (дабигатрана этексилат), ENTRUST (эдоксабан) и AUGUSTUS PIONEER-PCI (апиксабан). Первая работа с говорящим названием была посвящена ривароксабану. В ней был сделан важный шаг, указывающий на более высокую безопасность двойной терапии по сравнению с тройной, хотя и были использованы «заниженные» дозировки ривароксабана. Самым крупным исследованием с наиболее уникальным дизайном является AUGUSTUS. Оно включало 4600 пациентов, в том числе с ОКС, которым не проводилось чрескожное коронарное вмешательство (ЧКВ). В результатах исследования сообщается не только о повышенных геморрагических рисках на фоне приема Аспирина, но и о преимуществах в безопасности апиксабана над варфарином.
Двойная антитромбоцитарная терапия после инфаркта. Сохраняющийся риск сосудистых осложнений и эффективность длительной двойной антитромбоцитарной терапии после инфаркта миокарда
Информация только для специалистов в сфере медицины, фармации и здравоохранения!В статье рассматриваются данные о длительности сохранения риска и основной причине сосудистых осложнений у больных, перенесших острый коронарный синдром. Представлены предпосылки к продленному использованию двойной антитромбоцитарной терапии после инфаркта миокарда. Рассматриваются результаты крупного международного проспективного рандомизированного плацебо-контролируемого исследования PEGASUS-TIMI 54 по оценке эффективности и безопасности длительного применения сочетания ацетилсалициловой кислоты и блокатора P2Y12-рецептора тромбоцитов тикагрелора у больных с высоким риском тромботических осложнений атеросклероза в сроки от 1 до 3 лет поле перенесенного инфаркта миокарда. Анализируются оптимальные подходы к продленной двойной антитромбоцитарной терапии после инфаркта миокарда с учетом результатов исследования PEGASUS-TIMI 54, которые легли в основу современных клинических рекомендаций. В исследовании PEGASUS-TIMI 54 продемонстрирована польза продления двойной антитромбоцитарной терапии как минимум до 4 лет после инфаркта миокарда у больных с высоким риском атеротромботических осложнений и установлена целесообразность уменьшения дозы тикагрелора с 90 до 60 мг 2 раза в сутки через 1 год после начала заболевания для обеспечения наилучшего соотношения эффективности и безопасности лечения. Возможность продления двойной антитромбоцитарной терапии с использованием сочетания АСК и тикагрелора в дозе 60 мг 2 раза в сутки через 1 год после инфаркта миокарда предусмотрена в инструкции по медицинскому применению тикагрелора и закреплена в существующих клинических рекомендациях. На сегодняшний день тикагрелор – единственный ингибитор Р2Y12-рецептора тромбоцитов, одобренный в Российской Федерации как дополнение к АСК при длительной профилактике атеротромботических сердечно-сосудистых событий.
Двойная антитромбоцитарная терапия после стентирования. Продолжительность двойной антитромбоцитарной терапии: спорные вопросы и возможные решения
З.М. Сафиуллина, Л.А. Сальникова, С.В. Шалаев
ГБОУ ВПО «Тюменский государственный медицинский университет» Минздрава РФ, Центр сердца и сосудов ГБУЗ Тюменской области «Областная клиническая больница № 1», г. ТюменьШирокая распространенность и высокая эффективность малоинвазивных коронарных вмешательств, в т. ч. коронарного стентирования, при различных формах ишемической болезни сердца диктует необходимость разработки действенных методов профилактики тромбозов стентов. В статье рассматриваются исследования последних лет, посвященные данной проблеме, оценивается влияние двойной антитромбоцитарной терапии различной продолжительности на сердечно-сосудистые и геморрагические осложнения у пациентов с острым коронарным синдромом и стабильной ИБС. Анализируется проблема предпочтительности выбора и продолжительности терапии дезагрегантами.
Впоследние годы актуальность разработки действенных методов профилактики тромбозов стентов возрастает в связи с широкой распространенностью и высокой эффективностью малоинвазивных коронарных вмешательств, в т.ч. коронарного стентирования (КС), при различных формах ишемической болезни сердца (ИБС). Совершенствование техники имплантации стентов и введение режима двойной антиагрегационной терапии значительно снизили частоту этого осложнения: c 16±0,4 до 2,8±1,2% .
Двойная антитромбоцитарная терапия (ДАТТ), включающая ацетилсалициловую кислоту (АСК) в комбинации с ингибиторами рецепторов P2Y12 (клопидогрел, прасугрел или тикагрелор), – эффективный метод лечения больных как острым коронарным синдромом (ОКС), так и стабильной ИБС, подвергаемых плановым чрескожным коронарным вмешательствам. Выбор второго антиагреганта определяется степенью доказанности в конкретной клинической ситуации, что отражено в современных клинических рекомендациях .
Согласно существующим рекомендациям, применение ДАТТ (АСК+ингибитор рецепторов P2Y12) является важным аспектом в профилактике тромбозов стентов. Рекомендованная длительность такого лечения составляет до 12 месяцев после имплантации стента при различных формах ОКС.
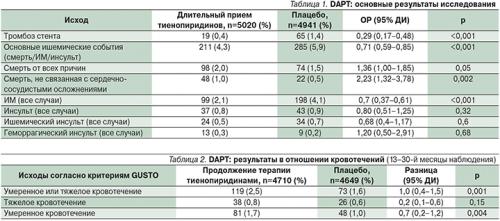
Однако результаты нового международного рандомизированного контролируемого клинического испытания DAPT продемонстрировали определенные преимущества более длительной ДАТТ. В исследовании были проанализированы данные более 20 тыс. пациентов с ИБС и КС с лекарственным покрытием, предназначенным для профилактики рестенозов. На протяжении первых 12 месяцев после КС все участники принимали АСК и тиенопиридин (65% пациентов – клопидогрел; 35% – прасугрел). После первых 12 месяцев пациентов, у которых не регистрировали тяжелых кардиоваскулярных событий или кровотечений, распределили в две группы: получавшие АСК+ингибитор рецепторов P2Y12 или АСК+плацебо. Этот курс лечения составил 18 месяцев.
В ходе проведения исследования дополнительное применение ингибитора рецепторов P2Y12 с 13-го по 30-й месяц значительно снизило вероятность возникновения тромбоза стента: инцидентность в группах тиенопиридина и плацебо составила 0,4 и 1,4% соответственно, относительный риск (ОР) – 0,29; 95% доверительный интервал (ДИ) – 0,7–0,48; p
В группе ингибитора рецепторов P2Y12 по сравнению с плацебо достоверно реже отмечены сердечно-сосудистые и цереброваскулярные осложнения в целом (смерть/ИМ/инсульт) – 4,3 и 5,9% соответственно (ОР – 0,71; 95% ДИ – 0,59–0,85; p
Более длительный прием ДАТТ ассоциировался с повышением частоты геморрагических событий, однако частота массивных и/или фатальных кровотечений различалась между группами недостоверно (табл. 2). Частота возникновения умеренных и тяжелых кровотечений (согласно критериям GUSTO) в группе тиенопиридина была достоверно выше, чем в группе плацебо, – 2,5 и 1,6% соответственно (ОР – 1,61; 95% ДИ – 1,21–2,16; p=0,001).
В процессе наблюдения с 13-го по 30-й месяц частота смерти от всех причин составила 2% в группе продолжения терапии тиенопиридином и 1,5% в группе плацебо (ОР – 1,36; 95% ДИ – 1,00–1,85; p=0,05), что стало неожиданным фактом; эти данные исследователи связывали с возможным неодинаковым распределением между группами пациентов с онкологическим заболеванием в анамнезе.
В подтверждение этой гипотезы результаты мета-анализа 14 рандомизированных контролируемых исследований с включением 69 644 пациентов не выявили достоверного повышения риска кардиоваскулярной (ОР – 1,01; р=0,81) и некардиоваскулярной (ОР – 1,04; р=0,66) смертности, смертности от всех причин (ОР – 1,05; 95% ДИ – 0,96–1,19; p=0,33) при ДАТТ длительностью более 12 месяцев по сравнению с более короткой продолжительностью ДАТТ или приемом одного аспирина.
В целом в исследовании DAPT общая смертность в группе тиенопиридина была выше, чем в группе плацебо (2,3 и 1,8%), но различия были на границе статистической значимости (ОР – 1,36; р=0,04). В группе тиенопиридина регистрировали больше летальных исходов, связанных с кровотечениями (11 против 3; p=0,06), фатальной травмой (7 против 2; p=0,07) и раком (31 против 14; p=0,02). Таким образом, некардиоваскулярная смертность в группе тиенопиридина и плацебо составила соответственно 1,1 и 0,6% (ОР – 1,80; p=0,01).
Следует учитывать, что увеличение числа ишемических событий было наиболее выражено в первые 3 месяца после прекращения применения тиенопиридинов независимо от длительности приема, что свидетельствует о возможной целесообразности более длительной терапии, особенно для пациентов с высоким риском сердечно-сосудистых осложнений.
Был проведен анализ результатов отдельной группы участников исследования DAPT – пациентов, которым был установлен стент с паклитакселем Taxus, получавших прасугрел. Данный анализ был представлен как отдельное исследование TL-PAS. Оказалось, что в данной группе пациентов отмечено более выраженное снижение частоты ишемических событий при более длительном приеме ДАТТ (ОР – 0,41; p
Таким образом, применение ДАТТ более года, с одной стороны, снижает риск возникновения тромбоза стента и сердечно-сосудистых осложнений, с другой – ассоциируется с повышенным риском кровотечений.
В противоположность полученным в DAPT данным, результаты нескольких проведенных ранее исследований обосновали наметившиеся тенденции к уменьшению длительности назначения ДАТТ после имплантации стентов с покрытием лекарственным препаратом с 12-го по 6-й и даже 3-й месяцы.
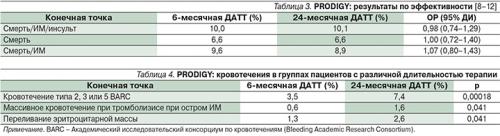
В исследовании PRODIGY 2 года ДАТТ после КС были не более эффективными, чем 6 месяцев лечения, в отношении ишемических осложнений, но при этом удвоилось число случаев массивных кровотечений (при исследовании продленной ДАТТ после стент-индуцированной гиперплазии интимы). Эти результаты позволили Марко Вальгимигли сделать следующее заявление: «Так как мы не можем исключить возможность того, что преимущества длительной терапии с применением клопидогрела на протяжении нескольких месяцев после КС могут быть меньше, чем ожидалось, то в нашем исследовании четко отражено, что отношение выгоды длительной терапии к риску было переоценено» .
Всего в исследование были включены 2013 пациентов: из них 74% – с ОКС и 26% – со стабильной стенокардией, которые перенесли КС и были рандомизированы для применения ДАТТ (клопидогрел+АСК на протяжении 6 и 24 месяцев). Первичной конечной точкой были общая смертность, повторный ИМ или инсульт в течение 2 лет. Общий риск первичной конечной точки был почти идентичным для обеих групп (табл. 3). При анализе ишемических событий в группах, в которых использовались разные типы стентов, различий не наблюдалось.
Существовали значимые различия между двумя группами с разной длительностью ДАТТ по числу пациентов с кровотечениями (табл. 4).
Cреди ограничений исследования PRODIGY следует отметить его открытое проведение, а также относительно небольшое число включенных пациентов. К достоинствам исследования можно отнести отсутствие спонсорской поддержки со стороны промышленности, вовлечение всех пациентов, желающих пройти лечение с использованием стентов (в т.ч. с ОКС и подъемом сегмента ST), использование непокрытых металлических стентов, а также высокий уровень приверженности лечению. Если в результате предыдущих исследований (PCI-CURE и CREDO) уже было установлено, что терапия с использованием клопидогрела продолжительностью до года является лучшим решением, нежели одномесячное КС с использованием непокрытого стента, то в исследовании PRODIGY проведено сравнение лечения пациентов длительностью от шести месяцев до двух лет с использованием непокрытого металлического стента и стента с лекарственным покрытием.
В двух других исследованиях, REAL-LATE и EXCELLENT, получены сходные с PRODIGY результаты, которые также не выявили преимуществ от длительной ДАТТ . Таким образом, в трех исследованиях были получены схожие результаты: длительная ДАТТ (до двух лет) не обнаружила клинических преимуществ в отношении сердечно-сосудистых осложнений, при этом четко отмечались признаки повышенной частоты кровотечений.
В исследованиях ISAR-SAFE и ITALIC также не было выявлено достоверных различий частоты ишемических и геморрагических событий между группами ДАТТ в течение 6 месяцев и дольше. Ограничением для обоих исследований стало следующее обстоятельство: они были прекращены досрочно в связи с проблемами набора пациентов и низким уровнем регистрируемых событий, однако авторы в обоих случаях сделали вывод, согласно которому 6-месячный прием ДАТТ не уступает более длительной терапии, особенно для пациентов с низким риском сердечно-сосудистых осложнений и наличием факторов риска кровотечений.
В исследовании ISAR-SAFE пациентов рандомизировали в группы 6- и 12-месячной терапии клопидогрелом после имплантации стента с покрытием лекарственным препаратом. По результатам исследования не было выявлено различий между группами в достижении комбинированной первичной конечной точки – смерть/ИМ/тромбоз стента/массивные кровотечения, либо в частоте ишемических и геморрагических событий по отдельности.
В исследование ITALIC были включены пациенты с имплантированным стентом с покрытием лекарственным препаратом, рандомизированные в группы ДАТТ на протяжении 6 или 24 месяцев. Было выявлено отсутствие достоверной разницы между группами в отношении комбинированной точки, включившей смерть, ИМ, ургентную реваскуляризацию целевого сосуда, инсульт и массивное кровотечение в течение 12 месяцев после КС, даже у пациентов высокого риска после перенесенного ОКС.
В обзоре Т. Palmerini и соавт. сравнивали результаты краткосрочной (1 года) ДАТТ после имплантации стентов с лекарственным покрытием. Анализировали результаты 4 исследований, включивших 8180 пациентов, учли такие клинические исходы, как сердечная смерть, ИМ и определенный/возможный тромбоз стента. Краткосрочная ДАТТ по сравнению с долгосрочной характеризовалась аналогичным уровнем сердечно-сосудистых осложнений (ОР – 1,11; 95% ДИ – 0,86–1,43, p=0,44), но статистически значимо низким уровнем кровотечений (ОР – 0,66; 95% ДИ – 0,46–0,94; p=0,03).
В недавнем исследовании OPTIDUAL , включившем 1385 пациентов после имплантации стентов с лекарственным покрытием, продолжение ДАТТ клопидогрелом и АСК до 48 месяцев не показало преимуществ по сравнению с проведением терапии на протяжении 12 месяцев в отношении развития сердечно-сосудистых осложнений. Первичная конечная точка была комбинированной и включала сердечно-сосудистые осложнения и показатели безопасности: случаи смерти, ИМ, инсульта, крупных кровотечений. В отношении развития первичной конечной точки между группами с длительной (48 месяцев) ДАТТ и ДАТТ в течение 12 месяцев достоверной статистической разницы выявлено не было: 5,8 против 7,5% (ОР – 0,75; 95% ДИ – 0,5–1,28; p=0,17). Статистический анализ отдельных компонентов первичной конечной точки показал схожие результаты: смерть: ОР – 0,65 (95% ДИ – 0,34–1,22; p=0.18); ИМ: ОР – 0,67 (95% ДИ – 0,31–1,44; p=0,31); инсульт: ОР – 0,9 (95% ДИ – 0,22–2,18; p 0,53); крупные кровотечения: ОР – 0,98 (95% ДИ – 0,47–2,05; p=0,95).
Однако анализ post-hoc продемонстрировал на границе статистической значимости тенденцию снижения сердечно-сосудистых осложнений (смерть, ИМ, инсульт) в группе ДАТТ 48 месяцев по сравнению с группой ДАТТ 12 месяцев: 4,2 против 6,4% (ОР – 0,64; 95% ДИ – 0,4–1,02; p=0,06), при этом с увеличением длительности ДАТТ не отмечено увеличения частоты крупных кровотечений (соответственно 2 против 2%; p=0,95) или смертности от всех причин.
Таким образом, результаты исследования OPTIDUAL согласуются с таковыми исследования DAPT в отношении развития сердечно-сосудистых осложнений у пациентов после имплантации стентов с лекарственным покрытием.
В исследовании PEGASUS-TIMI 54 были рандомизированы 21 162 пациента с ОКС, разделенных на группы, принимавших тикагрелор 90 мг дважды в день, 60 мг дважды в день, и группу плацебо. Продолжительность наблюдения в среднем составила 33 месяца, продемонстрировано достоверное снижение таких сердечно-сосудистых осложнений, как сердечно-сосудистая смерть, ИМ или инсульт, на терапии тикагрелором 90 мг 2 раза в день по сравнению с плацебо (ОР – 0,85; 95% ДИ – 0,75–0,96; p
Заключение
Попытка сформулировать единую рекомендацию по длительности применения ДАТТ представляет большую сложность, поскольку результаты исследований различаются.
Вопрос о длительности ДАТТ определяется двумя основными задачами: защитой пациента от тромбоза стента и вторичной профилактикой сердечно-сосудистых осложнений в рамках существующей ИБС.
В отношении предотвращения тромбоза стента данные свидетельствуют о том, что ДАТТ на протяжении 6 месяцев безопасна в плане геморрагических осложнений, особенно для пациентов низкого риска ишемических осложнений с установленным современным стентом. При наличии у пациента более высокого ишемического риска более полезной может быть длительная ДАТТ, возможно даже на протяжении всей жизни, что подтверждают данные более ранних исследований – CREDO и TRILOGY ACS. Аналогичным образом большая часть преимуществ длительной ДАТТ, выявленных в исследовании DAPT, связана со снижением частоты ишемических событий, не ассоциированных с тромбозом стента, и это свидетельствует о том, что полученные результаты отражают в основном эффект в отношении вторичной профилактики. Европейские исследования ISAR-SAFE и ITALIC главной целью ставили изучение проблемы предотвращения событий, связанных с тромбозом стента у пациентов низкого риска. Эти работы, равно как и ранее проведенные исследования, продемонстрировали, что можно безопасно отменять ДАТТ после 6 месяцев приема, если у пациента есть факторы риска кровотечения.
Следует учитывать и другой факт: польза пролонгированной ДАТТ может зависеть от типа имплантированного стента. По результатам исследования DAPT было выявлено, что преимущество длительной ДАТТ в плане снижения частоты основных неблагоприятных кардио- и цереброваскулярных событий максимально для пациентов, которым были установлены стенты с паклитакселем (ОР – 0,52), а минимально – для пациентов, которым были установлены стенты с эверолимусом (ОР – 0,89; p=0,05). Бурное развитие и усовершенствование технологии производства стентов позволяет надеяться на прогресс в этой важной области кардиологии.
Таким образом, наиболее безопасная и наиболее эффективная длительность приема ДАТТ остается неопределенной и должна рассматриваться индивидуально для каждого пациента. В каждом отдельном случае нужно оценивать и подбирать длительность ДАТТ, исходя из наличия факторов, способствующих атеротромбозу, при одновременном учете риска кровотечений и типа имплантированного стента.
Двойная антиагрегантная терапия при окс. Обзор

Документ содержит великолепные наглядные алгоритмы по применению двойной антитромбоцитарной терапии в различных ситуациях.
Имеются главы:
- по двойной антитромбоцитарной терапии и чрескожным коронарным вмешательствам;
- по двойной антитромбоцитарной терапии и операциям на сердце;
- по двойной антитромбоцитарной терапии у пациентов с лекарственной терапией острого коронарного синдрома;
- по двойной антитромбоцитарной терапии у пациентов с показаниями для пер-оральной антикоагуляцией;
- по плановым не-кардиохирургическим операциям у пациентов, применяющих двойную антитромбоцитарную терапию;
- по двойной антитромбоцитарной терапии у отдельных категорий пациентов, включая женщин, сахарный диабет, а также у пациентов, у которых развивается кровотечение во время лечения.
Документ рекомендует использование прогностической модели по оценке риска кровотечения во время применения двойной антитромбоцитарной терапии, а также рекомендует индивидуализированных подход, основанный на соотношении риска ишемии к риску кровотечения.
Рекомендуется, что по умолчанию пациенты с острым коронарным синдромом должны получать двойную антитромбоцитарную терапию в течение 12 месяцев , вне зависимости от реваскуляризационной стратегии (лекарственная терапия, чрескожное коронарное вмешательство или аорто-коронарное шунтирование).
У пациентов с высоким риском кровотечения необходимо рассмотреть возможность применения двойной антитромбоцитарной терапии в течение 6 месяцев.
У пациентов с острым коронарным синдромом, которые хорошо перенесли двойную антитромбоцитарную терапию без осложнений в виде кровотечения, можно рассмотреть возможность двойной антитромбоцитарной терапии более 12 месяцев.
В документе подчеркивается, что необходимость в более короткой продолжительности двойной антитромбоцитарной терапии не должно становиться обоснованием к применению непокрытых металлических стентов вместо стентов нового поколения, выделяющих лекарственное средство.
Продолжительность двойной антитромбоцитарной терапии должна основываться на оценке соотношения риска ишемии к риску кровотечения, а не по типу стента.
Вне зависимости от типа имплантированного металлического стента, у пациентов со стабильной коронарной болезнью сердца, пролеченных чрескожным коронарным вмешательством, продолжительность двойной антитромбоцитарной терапии должна быть от 1 до 6 месяцев в зависимости от риска кровотечения. Можно рассмотреть возможность более длительной продолжительности двойной антитромбоцитарной терапии у пациентов, у которых ишемический риск превышает риск кровотечения.
Нет достаточных данных для рекомендации двойной антитромбоцитарной терапии у пациентов со стабильной коронарной болезнью сердца, пролеченных аортокоронарным шунтированием.
Добавление двойной антитромбоцитарной терапии к пероральной антикоагуляционной терапии повышает риск осложнений в виде кровотечений в 2-3 раза. Необходимо пересмотреть показания к пероральной антикоагуляции и продолжать лечение только при наличии убедительных показаний, таких как мерцательная аритмия, механический клапан сердца или недавний случай рецидивного тромбоза глубоких вен, либо ТЭЛА.
Продолжительность тройной терапии (двойная антитромбоцитарная терапия плюс пероральная антикоагуляция) должна быть ограничена 6 месяцами либо не применяться после выписки из стационара в зависимости от рисков ишемии и кровотечения.
Клопидогрел рекомендуется как ингибитор P2Y1,2 по умолчанию у пациентов со стабильной коронарной болезнью сердца, пролеченных чрескожным коронарным вмешательством, у пациентов с показаниями к пероральной антикоагуляции и у пациентов с острым коронарным синдромом, у которых имеются противопоказания к применению тикагрелора или прасугреля.
Тикагрелор или прасугрель рекомендуются для пациентов с острым коронарным синдромом, если только нет противопоказаний к их применению.
Одинаковый тип или одинаковая продолжительность двойной антитромбоцитарной терапии рекомендуется и мужчинам и женщинам, а также пациентам с или без сахарного диабета.
Подробнее об обновленном руководстве вы можете прочитать, скачав прикрепленный файл.
Двойная антиагрегантная терапия при инсульте. Инсульт и ТИА
Антитромботическая стратегия в остром периоде ИИ основывается на применении тканевых активаторов плазминогена (tPA) в кратчайшие сроки после появления первых симптомов ОЦИ. Кроме тромболитической терапии, АСК в суточной дозе 81-325 мг оказывает существенное влияние на исходы, если препарат назначен в первые 48 часов (класс I, уровень А). Другие антитромботические средства (антикоагулянты или антиагреганты) не рекомендованы в остром периоде ИИ в связи с высокой вероятностью кровотечений, в том числе в области ишемического очага . Препараты АСК назначают в качестве единственного антитромботического средства как можно раньше или через 24 часа после проведения тромболизиса. Внутривенная тромболитическая терапия (вТЛТ) является наиболее эффективным и перспективным методом лечения больных с ИИ. Однако в реальной клинической практике вТЛТ получают менее 10% больных.
Это связано с проблемами организации неотложной помощи и многочисленными противопоказаниями к проведению этого метода лечения. Следовательно, АСК является единственной альтернативой вТЛТ для большинства больных. Метаанализ сравнительной эффективности и безопасности АСК (48 часов) и вТЛТ (4,5 часа) показал, что количество больных с хорошим функциональным исходом после тромболизиса увеличивается в 10 раз. Более вероятный хороший функциональный исход – это и есть преимущество вТЛТ, для которого предпринимаются активные усилия по организации медицинской помощи больным в специализированных сосудистых центрах. Однако и АСК оказывает заметное влияние на исходы ОНМК. АСК в остром периоде ИИ на 5% снижает летальность и оказывает существенное влияние на частоту повторных сосудистых событий . АСК ассоциируется с незначительным увеличением числа внутричерепных кровоизлияний. ТЛТ увеличивает вероятность кровоизлияния в мозг или клинически значимой геморрагической трансформации ишемического очага в 25 раз. В целом для больных с ИИ АСК полезна и безопасна как в качестве основного антитромботического средства, так и после ТЛТ.
Антитромботическая стратегия в остром периоде ИИ основывается на применении тканевых активаторов плазминогена (tPA) в кратчайшие срок после появления первых симптомов ОЦИ. Кроме того, АСК в суточной дозе 81-325 мг оказывает существенное влияние на исходы, если препарат назначен в первые 48 часов (класс I, уровень А).
Другие антитромботические средства (антикоагулянты или антиагреганты) не рекомендованы в остром периоде ИИ в связи с высокой вероятностью кровотечений, в том числе в области ишемического очага.
Препараты АСК назначают в качестве единственного антитромботического средства как можно раньше или через 24 часа после проведения тромболизиса.
Внутривенная тромболитическая терапия (вТЛТ) является наиболее эффективным и перспективным методом лечения больных с ИИ. Однако в реальной клинической практике вТЛТ получают менее 10% больных.
Это связано с проблемами организации неотложной помощи и многочисленными противопоказаниями к проведению этого метода лечения. Следовательно, АСК является единственной альтернативой вТЛТ для большинства больных.
Метаанализ сравнительной эффективности и безопасности АСК (48 часов) и вТЛТ (4,5 часа) показал, что количество больных с хорошим функциональным исходом после тромболизиса увеличивается в 10 раз.
Более вероятный хороший функциональный исход – это и есть преимущество вТЛТ, для которого предпринимаются активные усилия по организации медицинской помощи больным в специализированных сосудистых центрах.
Однако и АСК оказывает заметное влияние на исходы ОНМК. АСК в остром периоде ИИ на 5% снижает летальность и оказывает существенное влияние на частоту повторных сосудистых событий.
АСК ассоциируется с незначительным увеличением числа внутричерепных кровоизлияний. ТЛТ увеличивает вероятность кровоизлияния в мозг или клинически значимой геморрагической трансформации ишемического очага в 25 раз.
В целом для больных с ИИ АСК полезна и безопасна как в качестве основного антитромботического средства, так и после ТЛТ.